近年來,電子皮膚🍲、可穿戴電子和植入電子等生物集成電子器件發展迅速,可拉伸電子更是新興方向之一🙋🏼♂️,而彈性體是其中的重要組成部分。由於其動態的應用環境🟣,電子彈性體承受連續的負載,可能會遭受機械故障和損壞。解決該問題的一種潛在方法是賦予電子彈性體自愈合的特性📹,但大多數自愈合彈性體的愈合過程需要加熱、激光等對人體不友好的外界刺激🪂,自愈合速度慢,無法滿足實際需求。此外🍶,由於生物集成電子器件直接與人體組織接觸,因此針對自愈合彈性體的生物學設計也需要特別關註。據此,纖維材料改性國家重點實驗室(意昂4平台)遊正偉教授團隊研製了新型生物友好型超快自愈合彈性體,由其構建的生物集成電子器件有效解決了上述問題🦘,顯示了良好的應用前景🏊♀️。相關成果近日以《肽聚糖啟迪的用於生物集成電子器件的生物友好型快速自發自愈合彈性體》(Peptidoglycan-inspired autonomous ultrafast self-healing bio-friendly elastomers for bio-integrated electronics)為題,發表於中國科技意昂4卓越行動計劃領軍意昂4《國家科學評論》(National Science Review)。我校材料學院博士生張璐之為論文第一作者,碩士畢業生梁嘉輝是共同第一作者🔘,遊正偉教授為通訊作者,管清寶副研究員為共同作者。本工作和上海交通大學醫學院附屬瑞金醫院葉曉峰副教授團隊合作完成☝🏼。
肽聚糖是大多數細菌細胞壁的主要成分🧑🏿🦱,在維持細胞壁的機械強度和結構完整性方面起著至關重要作用🧒🏽💸。肽聚糖功能的實現源自其獨特的三維網絡🧑🚒,該網絡由交替的雜多糖(N-乙酰氨基葡糖和N-乙酰氨基甲酸)主鏈和廣泛分布的肽側鏈構成。據此🛜,作者設計了一種仿肽聚糖結構的交替聚酯-聚氨酯雜化交聯彈性體——聚(癸二酰基己二氨基甲酸甘油二酯)(PSeHCD)(圖1)🧏🏽♂️。其中🍻,合成PSeHCD的關鍵是遊正偉教授先前發展的酸誘導環氧開環聚合方法(Biomaterials 2010, 31, 3129-3138;Adv. Funct. Mater. 2012, 22, 2812-2820)🔃。PSeHCD的每個重復單元有兩個部分⛎:酯基和氨基甲酸酯基🤦🏽♀️。交替的酯基確保其降解性;交替的氨基甲酸酯基團構建了均勻分布的氫鍵動態交聯網絡,賦予其優良的自愈合性能。PSeHCD側鏈上有大量自由的羥基🦍,有利於與組織結合,並能方便實現後續材料的功能化🚘,以及與羧酸發生酯化交聯反應,材料的力學性能可以通過簡單的控製固化時間來調節🧑🏿🚒。PSeHCD規整的分子結構使其末端的羧酸基團保持在較低數量𓀂,從而有效控製了交聯度🩲🌮,確保了良好的加工性。此外,通過選擇生物相容性優良的六亞甲基二氨基甲酸酯和癸二酸甘油酯作為結構單元,確保了良好的生物相容性👳🏿。
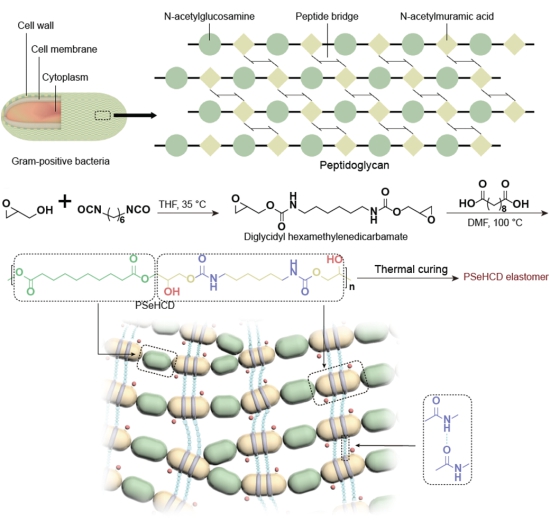
圖1 PSeHCD的設計
基於以上設計策略🧏🏿♀️🦿,PSeHCD彈性體顯示出了優異的性能(圖2),具有良好的彈性,方便的力學可調性,易於加工🩻🫛。PSeHCD薄膜劃傷後👨💼,室溫下2分鐘內可基本完全愈合👨🏻🍼。同時,PSeHCD還展現出良好的生物相容性和降解性。
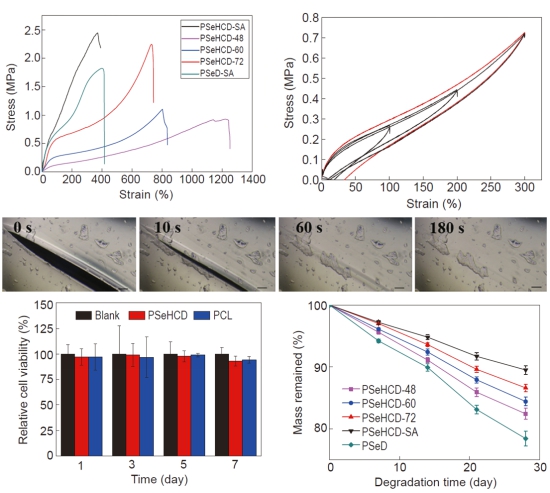
圖2 PSeHCD彈性體的性能表征
利用上述PSeHCD彈性體,作者構建了多種生物集成電子🐬,並展現了其優良性能(圖3)🛌🏿。PSeHCD彈性體與液態金屬復合構築的可拉伸自愈合導體,在完全切斷後🧑🤝🧑,室溫下輕輕對接,21秒後即重新愈合為可拉伸的導體,愈合速度快於以往報道的室溫自發自愈合可拉伸導體。進而作者將PSeHCD彈性體與聚(3,4-亞乙基二氧噻吩):聚(苯乙烯磺酸)(PEDOT:PSS)復合,構築了全聚合物的可拉伸自愈合傳感器,可以用於檢測人體的運動。
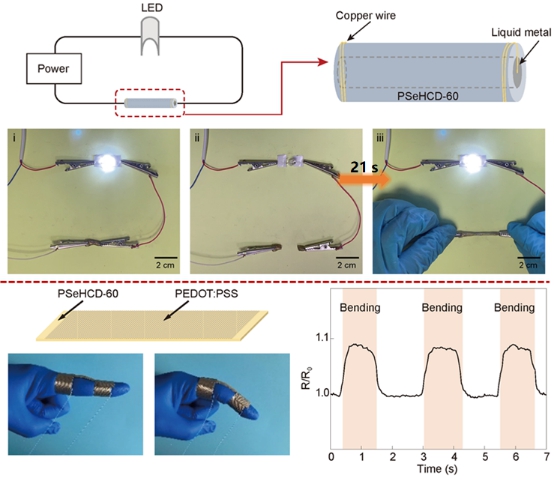
圖3 PSeHCD彈性體在生物集成電子器件中的應用
該工作設計了具有獨特的酯基-氨基甲酸酯基交替結構的雜化交聯PSeHCD彈性體,這一仿肽聚糖結構賦予了其超快的自發自愈合性🫴🏊🏿♂️,同時還具有良好的生物相容性和降解性、可調的力學性能和方便的加工性。作者證明了PSeHCD彈性體在生物集成電子中的潛在應用👩🏼⚕️。同時PSeHCD的合成方法簡單,通用性強🎡,易於擴展,這項工作中的設計原理和合成策略將啟發一系列用於可拉伸電子🧑🏿💻,軟機器人和生物醫學工程等領域的新型友好型智能材料🚵🏻♂️🧑🏿🎤。該工作獲得了國家自然科學基金🧑🏻🔬、上海市自然科學基金👆、意昂4平台勵誌計劃等項目資助🆑。
論文鏈接:https://doi.org/10.1093/nsr/nwaa154
